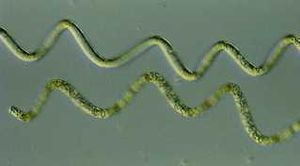
Spirulina
Spirulina-Produkte sind Nahrungsergänzungsmittel und werden aus der Cyanobakterie (Blaualge) Spirulina platensis gewonnen. Es handelt sich dabei rechtlich gesehen um Lebensmittel, die dem LFGB-Gesetz unterliegen. Ein gesundheitlicher Nutzen einer Einnahme von Spirulina ist wissenschaftlich nicht nachgewiesen.
Systematik
Bei Spirulina platensis-Produkten (landläufig als Spirulina-Algen beworben; lat. Arthrospira platensis) handelt es sich wie auch bei den Afa-Algen um Cyanobakterien (Eubakterien). Wie andere so genannte "Mikroalgen" zeichnen sich diese Bakterien dadurch aus, dass sie lange Ketten bilden können und auf diese Weise eine den Algenpflanzen ähnliche Struktur zeigen. Spirulina bildet, wie der Name bereits andeutet, spiralig gewundene Ketten.
Inhaltsstoffe
Trockenpräparate aus Spirulina enthalten durchschnittlich:[1][2]
- 59,78% Proteine
- 20,2% Kohlenhydrate
- 4,06% Fette, hier vor allem Gammalinolensäure
- 5,47% Mineralstoffe (Kalzium, Eisen, Magnesium, Natrium, Zink)
Das in den Produkten enthaltene Vitamin Vitamin B12 ist zu einem überwiegenden Teil in einer Form enthalten, die beim Menschen keinerlei Effekt ausübt oder die Serumspiegel dieser Vitamine nicht verändern kann. Deswegen wird es auch als Pseudovitamin B12 bezeichnet.[3]
So stellten Dagnelie et al. bei einem Kind mit Vitamin B12-Defizit fest, dass zwar die Serumspiegel nach Zufuhr von Spirulina anstieg, sich der Zustand der megaloblastären Anämie (mit vergrößertem mittleren Zellvolumen MCV) aber verschlechterte, was auf eine Unwirksamkeit der des Präparates schließen lässt. Im Gegensatz dazu verbesserte (normalisierte) sich das MCV nach Umstellung auf fischreiche Kost. Nach Ansicht dieser Autoren ist es nicht gerechtfertigt, Algen oder andere Pflanzenprodukte als sichere Vitamin B12-Quelle zu bezeichnen, da die tatsächliche Bioverfügbarkeit von Vitamin B12 aus diesen Ressourcen fraglich ist.[4]
Einsatzgebiete
Nahrung
Bereits die spanischen Conqistadoren sollen berichtet haben, dass die Azteken Spirulina als Nahrungsgrundlage verwendeten. Gesichert ist, dass das Volk der Kanembu Spirulina aus dem Tschad-See geerntet hat. Diese Nahrungsquelle diente offensichtlich in den genannten Kulturen dem Zweck der Nahrungsmittelversorgung in Notfällen oder als Beimischung zur Normalkost.
Nahrungsergänzungsmittel
Die Spirulina-Produkte werden zur Vorbeugung und Behandlung von Fibromyalgie, erhöhter Blutfettwerte, Krebsvorbeugung, gegen HIV- und Herpes-Infektion, geschwächter Immunabwehr, Allergien, Leberschäden und auch zur Gewichtsreduktion beworben. Klinische Studien, die die Wirksamkeit beweisen, liegen für die beworbenen Indikationen nicht bzw. für den Menschen nicht vor.
Tierfutter
In der intensiven Landwirtschaft gilt Spirulina als hochwertiger Proteinlieferant in der Hühner-[5] und Karpfenzucht[6] in Indien. Dort dient Spirulina platensis also als billige Proteinquelle in der Tierzucht, um teure pflanzliche Proteinquellen zu ersetzen. Spirulia ist Bestandteil einiger Futtermittel für Fische und Katzen.
Vermarktung
Im Internet und im Strukturvertrieb, aber auch über den Internetversand können die Mittel bezogen werden. Es kam bereits zu Verurteilungen von Spirulina-Anbietern auf Grund unlauterer Werbung.
Kultivierung und Ernte von Spirulina
Spirulina kommt natürlich in stark alkalischen Salzseen (pH-Wert zwischen 9 und 11) vor und besiedelt flache, subtropische bis tropische Gewässer mit hohem Salzgehalt, vor allem in Mittelamerika, Südostasien, Afrika und Australien.
Spirulina gedeiht nur unter warmen klimatischen Bedingungen innerhalb des Bereiches zwischen dem 35. Breitengrad nördlich bzw. südlich des Äquators. Außerhalb dieser Klimazone kann Spirulina nur in thermisch regulierten Aquakulturen bei einer Wassertemperatur von bis zu 35° Celsius kultiviert werden. Zur Ernte pumpt man das Wasser mit den Mikroorganismen durch einen Filter oder eine Zentrifuge und trocknet das so gewonnene Sediment anschließend mit Heißluft.
Da sich die einzelnen pflanzenartig wachsenden Bakterienstränge zusammenballen und schnell wachsend sind, kann man sie leicht ernten.
Spirulina platensis wird heute in der Regel industriell hergestellt, um auf dem Gesundheitsmarkt angeboten zu werden. Während man in Afrika, Asien und Südamerika die Produktion in kleinen Mengen dezentral bewerkstelligt, wird z.B. in den USA der Weg beschritten, Spirulina-Stämme zu isolieren und als Reinzucht in isolierten Tanks zu vermehren.
Wirksamkeit
Studien wie Pugh et al. (2001) deuten darauf hin, dass in Spirulina platensis, AFA-Algen (Aphanizomenon flos aquae) und Chlorella pyrenoidosa-Zubereitungen im Zellkulturversuch immunmodulatorisch wirksame hochmolekulare Polysaccharide in einem Anteil von 0,5-2% enthalten sind.[7] Diese führen in Zellkultur-Prüfmodellen zu einer Aktivierung menschlicher weißer Blutkörperchen (Monozyten, Makrophagen), die für die Immunabwehr zuständig sind. Daraus aber eine heilsame Wirkung beim Menschen abzuleiten, ist falsch. Verschiedene als Antigene wirkende Substanzen (bis hin zu reinem Wasser), können je nach Versuchsaufbau eine Aktivitätserhöhung bestimmter Zellfraktionen auslösen, weil eine Änderung der Laborbedingungen immer einen Einfluss auf die kultivierten Zellen ausübt. Selbst wenn im Serum des Menschen ein analoger Effekt zu erzielen wäre, würde dies lediglich bedeuten, dass die Zufuhr dieser Polysaccharide (deren Aufnahme aus dem Darm in das Serum bis heute nicht nachgewiesen wurde) wie eine Antigenzufuhr wirkt. Ein gesundheitlicher Nutzen entsteht dadurch nicht zwangsläufig.
Allerdings existiert bis heute keine einzige klinische Studie, die glaubhaft und seriös einen gesundheitlichen Vorteil der dauerhaften Einnahme von Spirulinaprodukten bei den behaupteten Indikationen nachwies.
Die Behauptung, Extrakte von Spirulina platensis seien gegen HIV/AIDS wirksam, ist bis heute unbewiesen. Es liegen nur wenige Laborstudien wie Ayehunie et al. (1998) vor, die zeigen, dass im Zellkulturversuch die HI1-Virus Vermehrung in menschlichen T-Zell-Linien durch einen wässrigen Auszug von Spirulina (Arthrospira) platensis in Konzentrationen von 0,2-1,2 Mikrogramm Extrakt pro ml Zellsuspension um etwa 50% hemmen kann.[8] Bis heute gibt es jedoch keine Studie und nicht einmal eine glaubwürdige Fallbeschreibung dazu, dass dieser Effekt bei HIV-Infizierten ebenso eintritt. Die Überlebenszeit von HIV-Infizierten, die sich zusätzlich mit Spirulina versorgen, wurde bis heute im Vergleich zu solchen Personen, die dies nicht tun, nicht untersucht. Es gibt also bis auf Zellkulturversuche keine verwertbaren Hinweis darauf, dass Spirulina bei HIV oder gar im symptomatischen Stadium AIDS einen therapeutischen Nutzen hat.
In der Behandlung der Adipositas gibt es bis heute keine Studie, die einen gewichtsreduzierenden Effekt auch nur untersuchte, geschweige denn einen Nutzen glaubhaft nachwies. Den einzigen angeblichen Nachweis bieten Becker et al.[9] in einer aufgrund ihrer Fallzahl faktisch nicht aussagekräftigen placebokontrollierten Studie in einem Journal der Lebensmittelindustrie.
Die Behauptung, dass Spirulina gegen Krebs vorbeugend schütze, ist bis heute nicht belegt. Zwar gibt es einige Zellkulturversuche, in denen wiederum immunmodulatorische Wirkungen von Spirulinaextrakten beschrieben wurden,[10] aber diese Versuche wurden nur bei gesunden Freiwilligen durchgeführt und zeigen den üblichen Anstieg der Natural Killer (NK)-Zellen im Serum bei der Zufuhr von oral resorbierbaren Antigenen. Es wäre falsch, daraus einen Anti-Tumor-Effekt ableiten zu wollen, da NK-Zellen nur immunologisch markierte Zellen angreifen und vernichten. Selbst wenn ihre Zahl im Serum drastisch erhöht würde, die Tumorzelle sich aber nicht als körpereigen darstellt (z.B. bei Adenokarzinom-Zellen), nutzt der Effekt einer NK-Stimulation dem Krebskranken überhaupt nicht. Eine spezielle Markierung oder Veränderung der Oberflächenstruktur von Tumorzellen durch die wässrigen Spirulina-Extrakte ist bis heute nicht nachgewiesen worden. Insofern sind solche Versuche immunologische Augenwischerei.
Es gibt allerdings Studien wie jene von Mishima et al. (1998), die das Polysaccharid Kalzium-Spirulan aus Spirulina platensis-Zubereitungen isolierten und im Zellkulturversuch als Hemmstoff in Zelllinien ausgewählter Melanom-, Kolonkarzinom- und Fibrosarkom-Linien anwendeten. Sie spritzen die Substanz in den Zellsud und stellten fest, dass die Polysaccharide eins von verschiedenen Anheftungsenzymen blockierten, die diese Tumorzellen benötigen, um sich während des Metastasierungsprozesses in gesunden Geweben festzusetzen. Dieser Effekt wurde aber bisher am lebenden Tier oder gar am Menschen nicht untersucht. Es wurden auch keine Fallbeschreibungen über heilende Wirkungen bei diesen Tumorarten veröffentlicht. Ebenso steht der Beweis aus, dass eine direkte, spezifisch die Tumorzellen eliminierende Wirkung des Kalzium-Spirulan existiert. Wenn überhaupt, kann es höchstens einen Teil der Anheftungskapazität bestimmter Tumorzellen bremsen und damit eine Metastasierung verlangsamen.[11]
Die einzige Studie, die bisher im Fachschrifttum publiziert wurde und sich mit der Spirulinabehandlung bei Kranken befasst, ist jene von Mathew et al. (1995) von der medizinischen Universität Kerala (Indien). Die Autoren untersuchten Veränderungen des Schleimhautepithels der Mundhöhle von Tabak kauenden Arbeitern. Es sollte untersucht werden, ob die 12-monatige Einnahme von 1 Gramm Spirulina platensis täglich einen Einfluss auf die Neigung zu Verhornungsstörungen (Leukoplakie) bei diesen Patienten hatte. 20 von 44 Patienten unter Spirulinagabe und nur 3 von 43 placebobehandelten Patienten zeigten eine Rückbildung der Leukoplakie im Mundhöhlenbereich. Eine Veränderung der Serumwerte von Retinol oder Betakarotin unter Spirulina-Einnahme wurde nicht festgestellt. Da es sich bei der Leukoplakie nicht um eine Krebserkrankung, sondern eine eventuell zu einem Mundhöhlenkarzinom führende Gewebsveränderung handelt, zeigt diese Studie, dass eine Wirkung bei Krebs nicht untersucht worden ist und offenbar das carotinoidreiche Spirulina keinen Einfluss auf den Vitaminspiegel im Serum hat. [12] Dies stützt die Beschreibung von Dagnelie et al. (1991), die ebenfalls keine Resorption von Vitaminen (hier: Vit. B12) feststellen konnten.
Zusammenfassend lässt sich sagen, dass eine medizinische Wirksamkeit wissenschaftlich nicht nachgewiesen werden konnte.
Gefahren
Durch schwermetallbelastete Produkte wie auch durch Spirulinaprodukte, die (möglicherweise durch Beimengungen microcystinproduzierender Cyanobakterien anderer Gattungen) Microcystine enthalten, besteht eine mögliche Gesundheitsgefährdung. Microcystine sind stark hepatotoxisch (giftig für die Leber) und gelten als Tumorpromotoren.[13]
In der Spirulina-Szene wird häufig die Legende verbreitet, dass die Produkte seien hochqualitativ, gerade weil sie im industriellen Maßstab unter Reinbedingungen erzeugt würden. Dass die resultierenden Produkte im Einzelfall alles andere als hochqualitativ sind, zeigte vor mehr als 15 Jahren die Studie von Johnson und Shubert (1986), die ergab, dass Schwermetalle aus verschmutztem Zuchtwasser zu einer Anreicherung von Blei, Kadmium und Quecksilber in den Endprodukten führen können.[14] Bei späteren Untersuchungen von Spirulina-Endprodukten fanden Nakashima et al. (1989) Beimengungen von Tierhaaren und Insektenfragmenten.[15] Zusätzlich waren die Produkte teilweise mit Mineralöl oder Reinigungsölen belastet. Dies deutet auf miserable Produktionsbedingungen einzelner Anbieter hin.
Spirulina platensis selbst enthält keine Microcystine. Jedoch werden oft andere Cyanobakterien, die zur Microcystinproduktion befähigt und mit Spirulina häufig vergesellschaftet sind, in angebliche Reinzuchtbecken eingeschleppt, die dann im Herstellungsprozess nicht abgetrennt werden. Je nach Seriosität und Zuverlässigkeit des Herstellers besteht dann die Gefahr, dass ein microcystinhaltiges Endprodukt in den Handel gelangt. So wurden bereits einzelne Spirulina-Produkte bekannt, die nachweislich Microcystine in Mengen bis zu 77 parts per billion (ppb) enthielten.
Bereits ab Belastungen von 30 ppb konnte eine Krebsgefahr (Leberkarzinom) nachgewiesen wurde[16][17] und im Versuch bei trächtigen Ratten schon ab einer Applikation von 4 ppb Microcystinen ins Bauchfell mikroskopisch erkennbare Organschäden der Rattenfeten gezeigt werden konnten[18], sind die gültigen Grenzwerte offenbar überdenkenswürdig.
Rechtliche Situation
Algenprodukte müssten in der Deutschland gemäß der EG-Verordnung Nr. 258/97 des Europäischen Parlaments und des Rates vom 27. Januar 1997 über neuartige Lebensmittel und neuartige Lebensmittelzutaten[19] laut Artikel 1 Abs. 2d als Lebensmittel und Lebensmittelzutaten aus Mikroorganismen, Pilzen oder Algen betrachtet werden. Da sie vor dem Jahr 1997 nicht in relevanter Menge im Verkehr waren, sind sie gemäß der Novel-Food-Verordnung zulassungspflichtig. [20]
In der Liste der beantragten und zugelassenen neuartigen Lebensmittel der EU sind keine Spirulina-Produkte aufgeführt.[21] Ebenso liegt keine Notifizierung über die Feststellung der wesentlichen Gleichwertigkeit mit anderen traditionellen Lebensmitteln vor. [22] Somit ist die Vermarktung solcher Produkte innerhalb der EU illegal.
Siehe auch
Weblinks
- Stiftung Warentest: Algenpräparate: Die grüne Gefahr test 02/2011 mit Video
- Barrett, Stephen: Algae: False Claims and Hype www.Quackwatch.com
Quellennachweise
- ↑ Tabelle der Hauptnährstoffe von Spirulina, getrocknet
- ↑ Clement G: Production and characteristic constituents of the algae Spirulina platensis and maxima. Ann Nutr Aliment 29: 477-88, 1975
- ↑ Watanabe F. et. al: Pseudovitamin B(12) ist he predominant cobamide of algal health food, spirulina tablets J Agric Fodd Chem. 1999 Nov;47(11):4736-41
- ↑ Dagnelie PC, van Staveren WA, van den Berg H: Vitamin B-12 from algae appears not to be bioavailable. Am J Clin Nutr 53: 695-697, 1991
- ↑ Venkataraman LV, Somasekaran T, Becker EW: Replacement value of blue-green alga (Spirulina platensis) for fishmeal and a vitamin-mineral premix for broiler chicks. Br Poult Sci 35: 373-81, 1994
- ↑ Nandeesha MC, Gangadhara B, Manissery JK, Venkataraman LV: Growth performance of two Indian major carps, catla (Catla catla) and rohu (Labeo rohita) fed diets containing different levels of Spirulina platensis. Bioresour Technol 80: 117-20, 2001
- ↑ Pugh N, Ross SA, ElSohly HN, ElSohly MA, Pasco DS: Isolation of three high molecular weight polysaccharide preparations with potent immunostimulatory activity from Spirulina platensis, aphanizomenon flos-aquae and Chlorella pyrenoidosa. Planta Med 67: 737-42, 2001
- ↑ Ayehunie et.al.: Inhibition of HIV-1 replication by an aqueous extract of Spirulina platensis (Arthrospira platensis) J Acquir immune Deficit Syndr Hum Retrovirol. 1998 May 1;18(1):7-12
- ↑ Becker EW, Jakober B, Luft D: Clinical and biochemical evaluations of the alga Spirulina with regard to its application in the treatment of obesity. A double-blind cross-over study. Nutr Rep Int 33: 565–574, 1986
- ↑ Hirahashi T, Matsumoto M, Hazeki K, Saeki Y, Ui M, Seya T: Activation of the human innate immune system by Spirulina: augmentation of interferon production and NK cytotoxicity by oral administration of hot water extract of Spirulina platensis. Int Immunopharmacol 2: 423-34, 2002
- ↑ Mishima T, Murata J, Toyoshima M, Fujii H, Nakajima M, Hayashi T, Kato T, Saiki I: Inhibition of tumor invasion and metastasis by calcium spirulan (Ca-SP), a novel sulfated polysaccharide derived from a blue-green alga, Spirulina platensis. Clin Exp Metastasis 16: 541-50, 1998
- ↑ Mathew B, Sankaranarayanan R, Nair PP, Varghese C, Somanathan T, Amma BP, Amma NS, Nair MK: Evaluation of chemoprevention of oral cancer with Spirulina fusiformis. Nutr Cancer 24: 197-202, 1995
- ↑ DFG - Senatskommission zur Beurteilung der gesundheitlichen Unbedenklichkeit von Lebensmitteln: Microcystine in Algenprodukten zur Nahrungsergänzung Endfassung vom 28. September 2005
- ↑ Johnson PE, Shubert LE: Accumulation of mercury and other elements by Spirulina (Cyanophyceae). Nutr Rep Int 34: 1063–1070, 1986
- ↑ Nakashima MJ, Angold S, Beavin BB, Bradicich RB, Decker SJ, Dzidowski GR, Levesque E, Locatelli RG, Mably M, Paredes A: Extraction of light filth from spirulina powders and tablets: collaborative study. J Assoc Off Anal Chem 72: 451-453, 1989
- ↑ Yu SZ: Primary prevention of hepatocellular carcinoma. J Gastroenterol Hepatol 10: 674-682, 1995
- ↑ Yu SZ, Chen G: Blue-green algae toxins and liver cancer. Chin J Cancer Res 6: 9-17, 1994
- ↑ Zhang Z, Lian M, Liu Y, Wei G, Yu S, Kang S, Zhang Y, Chen C: Teratosis and damage of viscera induced by microcystin in SD rat fetuses. Zhonghua Yi Xue Za Zhi 82: 345-347, 2002
- ↑ Amtsblatt Nr. L 043 vom 14/02/1997 S. 0001 - 0006
- ↑ http://ec.europa.eu/food/food/biotechnology/novelfood/nfnetweb/mod_search/index.cfm?action=mod_search.details&seqfce=45
- ↑ Applications under Regulation (EC) N° 258/97 of the European Parliament and of the Council
- ↑ Bundesinstitut für Risikobewertung (BfR): Notifizierungen neuartiger Lebensmittel gemäß Artikel 5 der Verordnung (EG) Nr. 258/97